تقدم جائزة نوبل سنويًا لمن ساهموا في تطوير الطب وتغيير العالم، منذ عام 1895. وقد أسسها مخترع الديناميت السويدي ألفريد نوبل، وأوصى بأن توزع الجوائز سنويًا لمن هم بحسب وصفه “جعلوا العالم مكانًا أفضل”. تمنح الجائزة في خمس مجالات وهي الطب، والكيمياء، والفيزياء، والأدب، والسلام. وقد بلغ عدد الجوائز في مجال الطب وعلم الوظائف الحيوية 114 جائزة بإضافة جائزة عام 2023. وقد حصل على جائزة نوبل في الطب 2023 كلًّا من الطبيبة كاتالين كاريكو والطبيب درو وايزمان من جامعة بنسلفينيا. منحت الجائزة لهما لاكتشافهما التعديلات الخاصة بقاعدة النيكلوزيد التي ساعدت في تطوير لقاحات الحمض النووي الريبوزي المرسال “mRNA” وهي التقنية التي استخدمت لتطوير لقاحات كوفيد-19.
استخدام mRNA في اللقاحات
عندما ظهر فيروس كوفيد-19 في نهاية عام 2019، كان من الصعب تخيل مدى سرعة تصنيع لقاح يتصدى لهذا الوباء للحد من انتشاره. ولكن في فترة قياسية، تمكن العلماء من تطوير العديد من اللقاحات. تلك السرعة دفعت البعض للاعتقاد بإنها مؤامرة، لذلك ظهرت بعض حملات رفض اللقاحات، لكنها عبرت عن جهل عامة الناس بتلك التقنية الجديدة فحسب. وقد تم اعتماد لقاحيين هما الأسرع والأكفأ في مواجهة الفيروس باستخدام تقنية الرنا المرسال mRNA الحديثة.
إن الظهور الأول لاستخدام تقنية الرنا المرسال كان منذ 30 عامًا تقريبًا، حيث كانت التجارب المخبرية تفيد بفعاليتها العلاجية. إلا أن تطبيقها سريريًّا تطلب التغلب على العديد من العقبات. كانت من ضمن تلك العقبات هي تحفيز الرنا المرسال للالتهابات غير المرغوب فيها أثناء عملية تحميل المادة الوراثية، وانتاجها بروتين غير فعال. إضافة إلى عدم ثبات واستقرار الرنا المرسال داخل الجسم الحي، لكونه جزيء هش يتحلل بسهولة بواسطة الإنزيمات الموجودة في الدم والأنسجة.
يصنع الرنا المرسال في المختبرات في عملية تسمى النسخ في المختبر in vitro transcription (IVT). تتم عملية IVT باستخدام إنزيم خاص يسمى بوليميريز RNA. يرتبط بوليميريز الرنا بقالب المادة الوراثية الأصلية الدنا وينسخه إلى رنا. ينسخ جزيء الحمض النووي الريبوزي (RNA) لينتج الرنا المرسال الذي سيتم استخدامه في اللقاح. يحتاج نقل الرنا المرسال إلى داخل الجسم الحي إلى ناقل ليحميه من التحلل داخل الجسم، لذلك استخدم العلماء عدة نواقل. من ضمنها النواقل الشحمية.
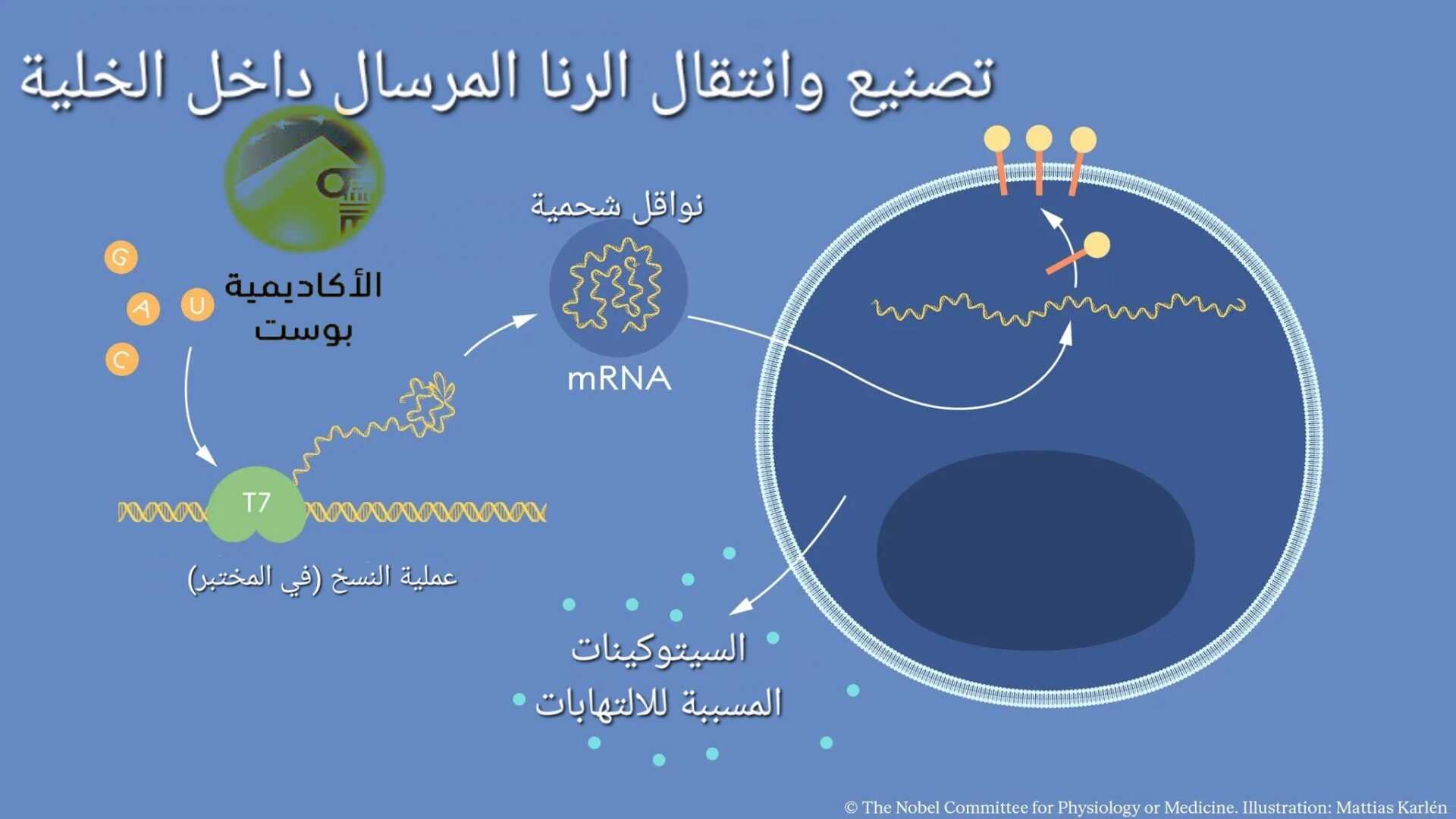
كانت نقطة التحول عندما اكتشفت كاريكو ووايزمان الرنا المرسال المعدل. تمكن الباحثان باستخدام الرنا المرسال المعدل من التغلب على العقبات عبر تجنب التعرف المناعي المسبب للالتهابات، وتحسين إنتاج البروتين. أدت تلك النتائج جنبًا إلى جنب مع تحسين وتطوير طرق استهداف الرنا المرسال لمناطق بعينها، وتثبيت واستقرار المستضد الخاص به في الجسم الحي إلى موافقة الجهات المختصة على اللقاح وتطبيقه سريريًّا على العامة. لتصبح مساهمة كاريكو ووايزمان ركيزة أساسية لبناء علم اللقاحات الشامخ في وقت شديد الحرج، وتمهيدًا لاستخدام تلك التقنية في المستقبل.
فيم تختلف اللقاحات قبل الوباء عن لقاحات الرنا المرسال؟
اعتمدت معظم اللقاحات الفيروسية قديمًا قبل لقاح الكوفيد على تقنية استخدام بروتينات فيروسية ضعيفة أو غير فعالة. تؤدي تلك البروتينات عملها عبر حقنها، فيكتسب الشخص مناعة عن طريق تكوين الخلايا التائية لأجسام مضادة للبروتينات الناتجة عن تلك الفيروسات. تتميز تلك اللقاحات بفعالية كبيرة ضد الفيروسات ولكنها تتطلب جرعات تحفيزية، بسبب ضعف الاستجابة المناعية بمرور الزمن.
كمرحلة ثانية، تطورت اللقاحات وأصبحت أكثر انتقائية بعد ثورة البيولوجيا الجزئية وتطوير تقنية إنتاج البروتينات، ليتم استخدام تلك التقنية والموافقة عليها لأول مرة في لقاح فيروس التهاب الكبد الوبائي عام 1986. ومن ثم لقاح الفيروسات المسببة للأورام في عام 2006. حيث يحتوي كلا اللقاحين على البروتين الخاص بكلا الفيروسين. ويشار إلى تلك اللقاحات باسم “لقاحات الوحدة الفرعية”. إذ تحمي تلك اللقاحات من تكون السرطانات مستقبلًا باستخدام مكونات بروتينية مؤتلفة.
وفي عام 2019، وكمرحلة ثالثة، استطاع العلماء تطوير لقاحات باستخدام هندسة الفيروسات البيولوجية، كما هو الحال في لقاح الإيبولا. إذ يعمل اللقاح عن طريق النواقل الفيروسية، حيث تقوم النواقل بإنتاج بروتين ذاتي لإنتاج مستضدات مشفر. تتمكن أجسادنا من التعرف على الفيروس عن طريق البروتين الخاص به ويشار إليها باسم “لقاحات النواقل”.
كلا التقنيتين السابقتين (المرحلة الثانية والثالثة) تحتاج إلى زراعة واسعة للخلايا لحقن المستضد الحقيقي، مما يحدّ من إمكانية إنتاج اللقاحات بشكل سريع في حالة التصدي للأوبئة. ولذلك طور الباحثون تقنية تتحايل على الحاجة إلى زراعة الخلايا الواسعة. حيث يمكن إيصال الحمض النووي عن طريق الرنا المرسال إلى المتلقي باستخدام إنتاج البروتين الزائف الخاص بالفيروس في المختبر بعد معرفة تسلسله الجيني. فيتحقق حلم الباحثين بإنتاج اللقاحات بشكل أسرع وتكلفة مادية أقل وهو ما يمثل نجاح هائل للمرحلة الرابعة.
كيف طُورت لقاحات الرنا المرسال؟
كانت بداية اللقاحات المعتمدة على الحمض النووي والرنا المرسال في بداية التسعينات. حيث تم اختبارها لأول مرة على الفئران، لتصبح بادرة أمل في عالم اللقاحات. على الرغم من صعوبة تصنيع اللقاحات القائمة على الحمض النووي، إلا أن مميزاتها شجعت على ذلك. إذ يمكن تعديل تسلسلها الجيني بسهولة لتكوين مستضدات مختلفة، كما يمكن إنتاج تلك اللقاحات بسهولة.
لقاحات الدنا DNA
وبالرغم من الاعتقاد بأن اللقاحات المعتمدة على الحمض النووي الدنا DNA ستكون أكثر فعالية عن تلك المعتمدة على الرنا المرسال. وذلك لكون الحمض النووي أكثر استقرارًا، لكن كان التطور في تلك اللقاحات بطيء. ولم تجرب سوى على فئران التجارب. يرجع السبب في ذلك إلى أن اللقاح المعتمد على الحمض النووي يحتاج إلى عبور حاجزين وهما غشاء البلازما، والغشاء النووي حول نواة الخلية للوصول إلى الحيز الخلوي لتحويل الحمض النووي إلى بروتينات. فعملية تحويل الحمض النووي إلى رنا مرسال والتي تسمى “عملية النسخ” تتم داخل النواة. وهو ما يصعب من استخدام الحمض النووي الدنا في اللقاحات.
الرنا المرسال المعدل
وبسبب صعوبة استخدام لقاحات الحمض النووي DNA أتت فكرة اللقاحات المعتمدة على الرنا المرسال، والتي لا تحتاج إلا لعبور حاجز واحد للوصول إلى السيتوبلازم. وفي السيتوبلازم، يتم تحويل الرنا المرسال إلى بروتين مباشرة. لماذا؟ لأن عملية ترجمة الرنا المرسال إلى بروتينات بالأساس تتم في سيتوبلازم الخلية ولا يحتاج في هذه الحالة الرنا المرسال إلى دخول النواة من الأساس. كما أن المعلومات الوراثية في تلك الحالة لن تندمج مع جينوم المتلقي، مما يوفر أمان عالي للخلايا البشرية خلال تلك العملية. بعبارة أخرى، لم يدخل الرنا المرسال المعدّل النواة من الأساس والتي تحتوي على المعلومات الوراثية الأصلية للكائن الحي. لم تحدث عملية تلاقي من الأساس بين المادتين الوراثيتين، بالتالي نسبة انتقال أو تلوث المادة الوراثية الأصلية بالمادة المحقونة تكاد تصل للصفر.
تطور نواقل لقاحات الرنا المرسال
إحدى عيوب اللقاحات الفيروسية المعتمدة على النواقل والتي ذكرناها في المرحلة الثانية والثالثة سابقًا، أنها تحفز الأجسام المضادة لمهاجمة البروتينات الهيكلية لتلك النواقل. مما يؤدي إلى هدم البنية البروتينية وتقليل استجابة الجسم لتلك النواقل إذا تم استخدام نفس النوع مرة أخرى. وقد نجح العلماء في تطوير لقاحات تستخدم نواقل فيروسية مطورة بتقنية هندسة الفيروسات الغدّية. واستطاعوا بذلك التصدى جزئيًا لجائحة كورونا السابقة خاصة في بدايتها.
ولأن مشكلة النواقل الفيروسية ستظل في حاجة لحلول جذرية، أصبح التحدي التالي يكمن في إيصال اللقاحات المعتمدة على الرنا المرسل داخل جسد الكائن الحي. في عام 1990، نشرت أول دراسة للعالم فيليب فلينجر وفريق عمله، تثبت أن حقن الرنا المرسال العاري، سمي بالعاري لأنه يخلو من النواقل، في العضلات الهيكلية قادر على إنتاج البروتين في الجسم الحي.
وقد أثبت مارتينون وفريق عمله بعد ذلك استجابات الخلايا اللمفاوية التائية السامة للخلايا الخاصة بمستضد معين في الفئران المحقونة بالرنا المرسال باستخدام جسيمات دهنية شحمية كنواقل. والجسيمات الشحمية هي جزيئات دهنية صغيرة تحيط بالرنا المرسال. تساعد الجسيمات الشحمية على حماية الرنا المرسال من التلف أثناء عملية التوصيل وعبور حواجز الخلية.
كما طور باحثون آخرون لقاحات النسخ المتماثل لفيروس ألفا، وهي لقاحات تعمل على إنتاج عدد أكبر بكثير من نسخ ترميز المستضد لكل خلية، مما قد يؤدي إلى استجابات مناعية أكثر قوة. ساعد نجاح هذا اللقاح في النسخ المتماثل لفيروس ألفا في النماذج الحيوانية على إظهار إمكانات لقاحات الرنا المرسال، ووضع الأساس لتطوير أول لقاحات تعتمد على الرنا المرسال ضد العدوى البشرية. ومن المهم أن نلاحظ أن تطوير لقاحات الرنا المرسال قد تم بعد تطوير الجسيمات الدهنية النانوية لتوصيل الرنا المرسال.
كاريكو وويزمان باحثان غيرا العالم
درس العالمان كاريكو وويزمان الأنواع المختلفة للحمض النووي الريبوزي ونشرا نتائج بحثهما في عام 2005. ولكن كان أصبح لاكتشافهما أهمية أكبر عندما ساعدا في تطوير لقاحات فيروس كورونا.
التغلب على الالتهاب
شرحت الدراسة تأثير تعديل قاعدة نيكلوزيد الرنا المرسال على استجابة السيتوكينات باستخدام الخلايا الجذعية. والسيتوكينات هي بروتينات تنتجها الخلايا وتساعد في تنظيم الاستجابة المناعية. وتلعب السيتوكينات دورًا مهمًا في الالتهاب والاستجابة المناعية وإصلاح الأنسجة. وقد أظهرت الدراسات أن الرنا المرسال والرنا الناقل في حقيقيات النواة لم يحفزا استجابة السيتوكينات. على خلاف الرنا المرسال في بدائيات النواة المنسوخة في المختبر، والتي استطاعت تحفيز السيتوكينات.
تم استخدام الخلايا الجذعية لدراسة تأثير تعديلات قاعدة الرنا المرسال على استجابة الخلايا الجذعية للالتهاب. وبدمج مركبات 5-ميثيل سيتيدين، أو N6-ميثيل أدينوزين، أو 5-ميثيلوريدين، أو 2-ثيوريدين في الرنا المرسال، وجد الباحثون أن هذه المركبات كانت قادرة على إلغاء تفعيل الاستجابات الالتهابية عند إضافة الرنا المرسال إلى الخلايا الجذعية.
كما تمكن الباحثون من عمل تعديلات على مركب اليريدين، وهو مركب يلعب دورًا مهمًا في تعديل قاعدة الرنا المرسال. هذه التعديلات أدت إلى إلغاء تنشيط التيار المستمر، وهو استجابة التهابية طويلة الأمد.
نتائج التعديل على الرنا المرسال
تشير النتائج إلى أن تعديلات قاعدة الرنا المرسال قد يكون لها آثار مهمة على تطوير علاجات جديدة للأمراض المناعية. على سبيل المثال، يمكن استخدام هذه التعديلات لمنع أو علاج الالتهاب المرتبط بأمراض مثل السرطان وأمراض المناعة الذاتية.
قبل أكثر من 40 عامًا لاحظ العالم إسحاق وفريقه، أن الحمض النووي الريبي المتحلل يمكنه تحفيز نوع من الانتروفين القوي لمواجهة الفيروسات. ولكن لم يستطع إسحاق معرفة كيفية وسبب ذلك. حتى أتى وايزمان وكاريكو بشرح ذلك في بداية الألفينات. والانتروفين هو نوع من السيتوكينات التي تعمل على مواجهة الفيروسات.
أوضحت الدراسات التي أجراها وايزمان وكاريكو لاحقًا السبب في استخدام اليردين المزيف (m1Ψ) بمفرده أو مع مركب 5-methylcytosine أنه يؤدي إلى تثبيط الاستجابة المناعية لتجنب الالتهابات غير المرغوب فيها وزيادة التعبير البروتيني. كما أن تلك التعديلات تجعل من الرنا المرسال أكثر استقرارًا داخل الخلية. تلك التعديلات هي الأكثر استخدامًا في اللقاحات الحديثة، بما في ذلك اللقاحين المستخدمين في مواجهة فيروس كورونا.
قام كاريكو وويزمان بحقن الرنا المرسال المعدل المحتوي على اليريدين المزيف في طحال فأر، لينتج كمية كبيرة من البروتين. ووجدوا أن بروتين PKR قد تم تنشيطه. وهو بروتين مضاد للفيروسات يمنع ترجمة البروتين. أظهر الفريق أن استخدام القواعد المعدلة للرنا المرسال يقلل من تنشيط PKR ويحسن إنتاج البروتين.
لقد ثبت أن استخدام m1Ψ في لقاحات الرنا المرسال آمن وفعال. وأظهرت التجارب السريرية تلك اللقاحات فعالة للغاية في الوقاية من الأمراض الخطيرة والاستشفاء والوفاة كما هو الحال مع كوفيد-19.
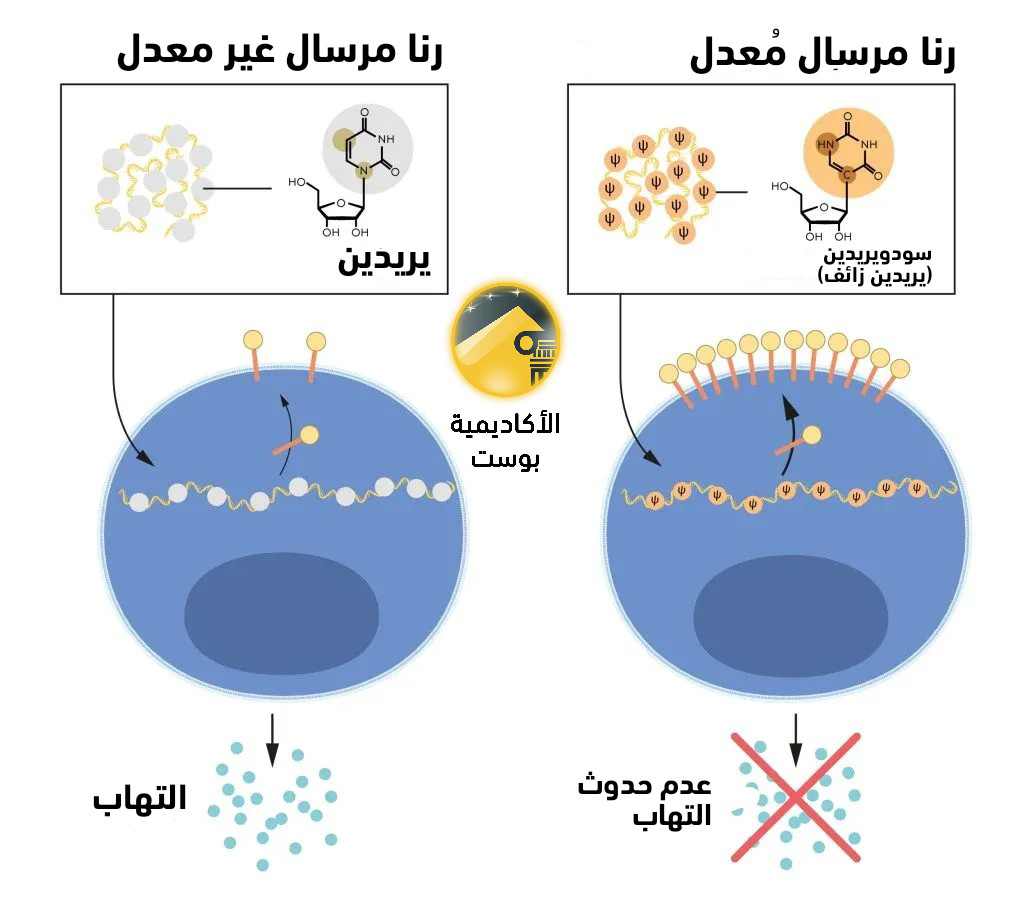
كيف بدأ انتاج لقاحات تعتمد على الرنا المرسال المعدل؟
بحلول عام 2010، تم تأسيس ثلاث شركات تعمل على تكنولوجيا الرنا المرسال وهم شركة CureVac، التي تأسست في عام 2000 بهدف تطوير لقاحات ضد الالتهابات والسرطان. وشركة BioNTech تأسست في عام 2008 بهدف تطوير لقاحات خاصة بالسرطان. وشركة Moderna، التي تأسست في عام 2010. استخدمت تقنية الرنا المرسال المعدل لإعادة برمجة الخلايا الجسدية إلى خلايا متعددة القدرات وتوصيل البروتينات العلاجية. وتعاونت الشركات الثلاث مع الباحثين لمواجهة الأمراض بتقنية حديثة آمنة وفعالة.
أثمرت جهود تلك الشركات بالتعاون مع العلماء والباحثين بالتصدي لبعض الفيروسات. منها فيروس زيكا في عام 2017. ومن ثم تعاونت شركة موديرنا مع العالم جراهام وفريقه للتصدي لفيروس كورونا القديم المتسبب لمتلازمة الشرق الأوسط التنفسية المعروف باسم سارس.
لقاحات كورونا المعتمدة على تقنية الرنا المرسال المعدل
بعد ظهور كوفيد-19 تعاونت تلك الشركات بالإضافة إلى شركات أخرى وعدد كبير من المؤسسات الأهلية والحكومات في بحث وتطوير وتمويل لقاح فيروس كوفيد-19. وتمت التجارب السريرية بالتوازي مع الأبحاث والتجارب المخبرية، وعلى غير المعتاد، حدثت بالتتابع نظرًا لحاجة العالم للقاح سريع. مما أدى إلى ظهور نتائج أسرع من العادة، حيث حصل كل من لقاحي الرنا المرسال المعدل من شركة Pfizer/BioNTech وModerna على الموافقة في غضون عام من تفشي فيروس كوفيد-19. أصبح هذا التطور ممكنًا بفضل عقود من البحث الأساسي وتحسين العمل على الرنا المرسال.
يحتوي كل من لقاحي الرنا المرسال من Pfizer/BioNTech وModerna على بدائل كاملة لليوريدين لتجنب الاستجابات الالتهابية غير المرغوب فيها، ولتكثيف ترجمة البروتين. أظهرت النتائج التي تم الحصول عليها بعد تطعيمين من الحمض النووي الريبوزي المرسال، أن مستوى الحماية ضد أعراض كوفيد-19 كان مرتفعًا للغاية. بفعالية 95% للقاح فايزر/بيونتيك (بولاك 2020) و94% للقاح موديرنا ( بادن 2021).
سرعان ما أظهرت الدراسات اللاحقة أن الاستجابة للقاح كانت قصيرة العمر نسبيًا. فتوصل مجتمع البحث العلمي أن التحصينات المعززة الإضافية حسنت الحماية بشكل كبير، خاصة ضد متحور أوميكرون الأكثر عدوى. وبعد عدة دراسات وتجارب أوضح المجتمع العلمي أن الأضرار الجانبية للقاحين كانت نادرة للغاية. مما يوفر فرصًا أكثر أمانًا للمزيد من التجارب والتطوير.
كيف سيساعد اكتشاف كاريكو ووايزمان الأطباء مرة أخرى؟
يجري الآن تطوير العديد من تطبيقات الرنا المرسال المعدل بالاعتماد على دراسة كاريكو ووايزمان. يشمل ذلك اللقاحات ضد الالتهابات وعلاج السرطان وتوصيل البروتينات العلاجية أو المعدلة للمناعة. من المؤكد أن تطوير تقنية الرنا المرسال هو لخدمة البشرية في التصدي للأمراض الأكثر خطورة أو انتشارًا كالأورام. وتُظهر الدراسات السريرية الحديثة لقاحات الرنا المرسال جنبًا إلى جنب مع علاجات تثبيط الورم باستخدام مستضدات الورم المتحولة أو غير المتحولة لتحفيز استجابات الخلايا التائية الخاصة بالورم في مرضى سرطان الجلد وسرطان القناة البنكرياسية.
يستخدم الرنا المرسال في هذه التجارب، ويعمل العلماء على تعديلات على ذيل poly(A) لزيادة ثبات الرنا المرسال وكفاءة تحويله إلى بروتينات. وبالتالي، هناك طرق بديلة لتوليد لقاحات وعلاجات فعالة تعتمد على الرنا المرسال قيد التطوير.
لم تحظ النتائج التي نشرتها كاريكو ووايزمان في بحثهما عام 2005 باهتمام كبير في حينها. ولكنها وضعت الأساس لتطوير اللقاحات التي خدمت العالم خلال جائحة كوفيد-19، ليستحقا جائزة نوبل في الطب لعالم 2023.
المصدر
سعدنا بزيارتك، جميع مقالات الموقع هي ملك موقع الأكاديمية بوست ولا يحق لأي شخص أو جهة استخدامها دون الإشارة إليها كمصدر. تعمل إدارة الموقع على إدارة عملية كتابة المحتوى العلمي دون تدخل مباشر في أسلوب الكاتب، مما يحمل الكاتب المسؤولية عن مدى دقة وسلامة ما يكتب.




التعليقات :