وضع العلماء عدة نماذج نووية لتفسير ظاهرة الإشعاع النووي التي تميز المواد المشعة عن غيرها من المواد المستقرة. وتصِف هذه النماذج الجسيمات، التي تكوِّن نواة الذرة، والتفاعلات التي تحدُث بينها. فما هي النماذج النووية؟ وإلى أي حد نجحت في تفسير ما يحدث داخل النواة؟
محتويات المقال :
النماذج النووية
تساهم النماذج النووية في فهم وتبسيط ما يحدث داخل النواة من ظواهر. فمنها ما يُشبِّه النواة ونوياتها (مكونات النواة) بقطرة ماء تتفاعَل داخلها جزيئات الماء، كما هو الحال في «نموذج قطرة السائل-Liquid-Drop Model». ومنها ما يُصورها على شكل غاز مضغوط في كرة بحجم نواة الذرة كما في «نموذج غاز فيرمي-Fermi gas model». وأخرى تعتبرها مكوَّنة من طبقات تختزن داخلها النويات المكوِّنة للنواة كما في «نموذج القشرة-The shell model » [1]. فسنستعرض بعض تلك النماذج هنا في هذا المقال.
1. نموذج متوسط الجهد
يُعد «نموذج متوسط الجهد» أساسًا لبعض النماذج الأخرى. وتخضَع النويات في هذا النموذج لجهد ثابت يبقيها مرتبطة فيما بينها داخل النواة. ينشَأ الجهد عن مختلف النويات التي تكوِّن النواة. وتسبَح كل نوية في متوسط هذا الجهد دون أن يكون لها أي ارتباط بباقي النويات، حيث يُعوِّض هذا الجهد التفاعل بين النويات الذي تم إهماله في هذا النموذج [1].
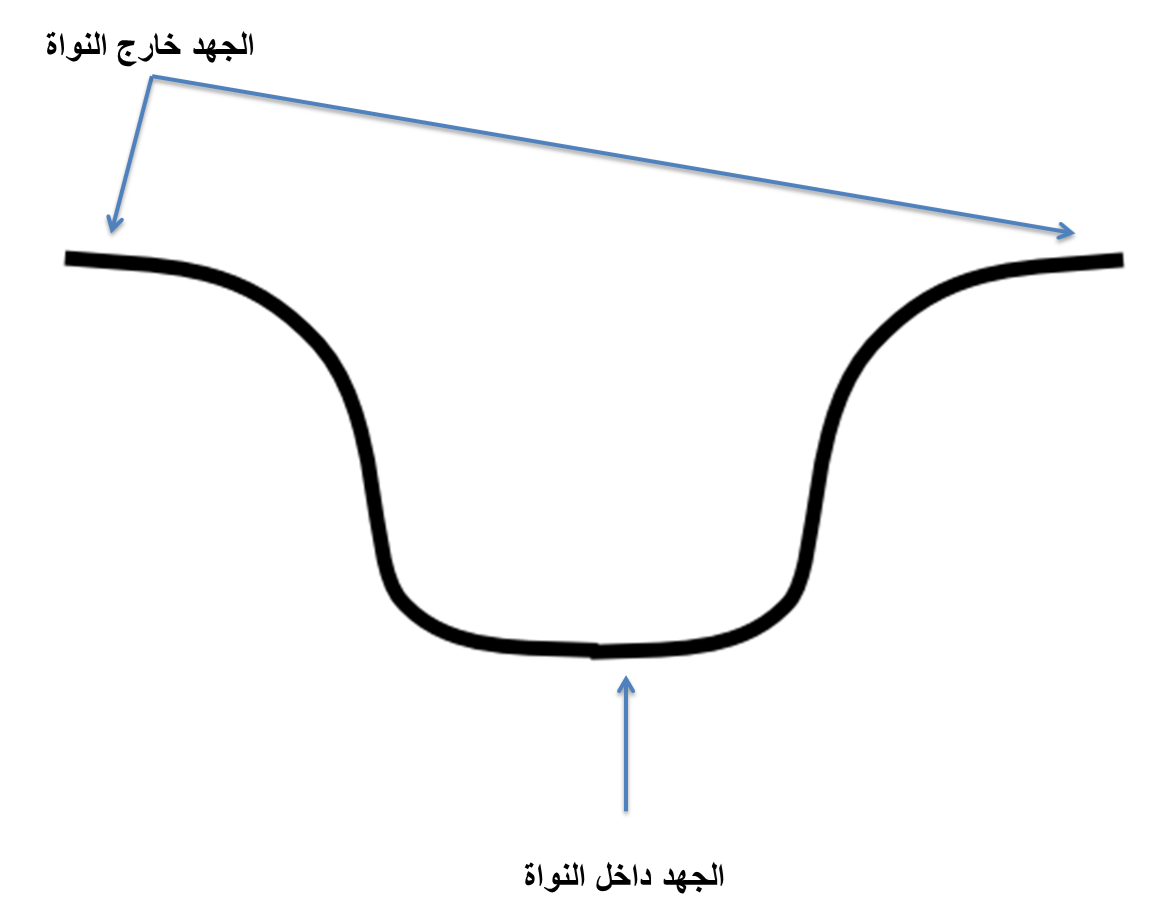
في هذا النموذج، تخضع البروتونات والنيوترونات (النويات المكونة للنواة) لـ «مبدأ الاستبعاد لباولي-Pauli exclusion principle» كل على حدة. ويفرض هذا المبدأ عدم إمكانية وجود بروتونين أو نيوترونين في نفس الحالة الكمومية (يجب أن يكون اتجاه الأسهم متعاكسًا كما هو مبين في الشكل 2) [1].
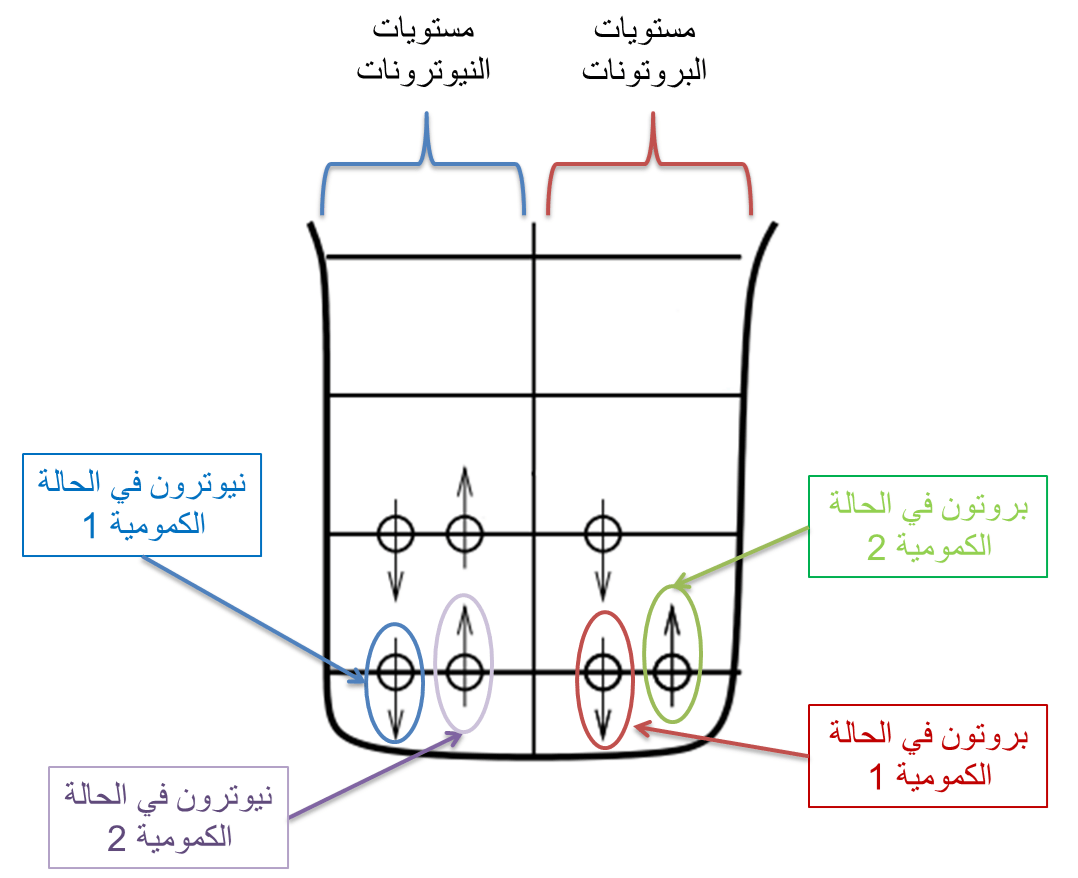
مستويات الطاقة
تسعَى النواة للحصول على الوضعية الأكثر استقرارًا، أي ذات مستويات الطاقة الأدنى. و تتوزع كل من البروتونات والنيوترونات على مستويات الطاقة بدءًا بالمستويات الأدنى نحو الأعلى مع احترام مبدأ الاستبعاد لباولي. ونتيجة لهذا، فإن النوى، التي يفُوق فيها عدد النيوترونات عدد البروتونات أو العكس، تحتَاج مستويات أعلى طاقة مقارنة بتلك التي يكون فيها عدد النيوترونات والبروتونات متساويًا، حيث يسهِم التفاوت بين البروتونات والنيوترونات إلى امتلاء مستويات الطاقة الخاصة بإحداها بينما تبقَى المستويات الدنيا للأخرى فارغة (انظر الشكل 3). فعلى سبيل المثال، بالنسبة لنواة تملك سبع نويات، نجد أن نواة البورون-7 أقل استقرارًا من نواة البريليوم-7، نظرًا لأن هذه الأخيرة تملك عددًا متقاربًا من البروتونات والنيوترونات (انظر الشكل 3). وهذا ما يفسر تحلل نواة البورون-7 إلى البريليوم-7 عن طريق التحلل b+ الذي يحول بروتونًا إلى نيوترون [1].
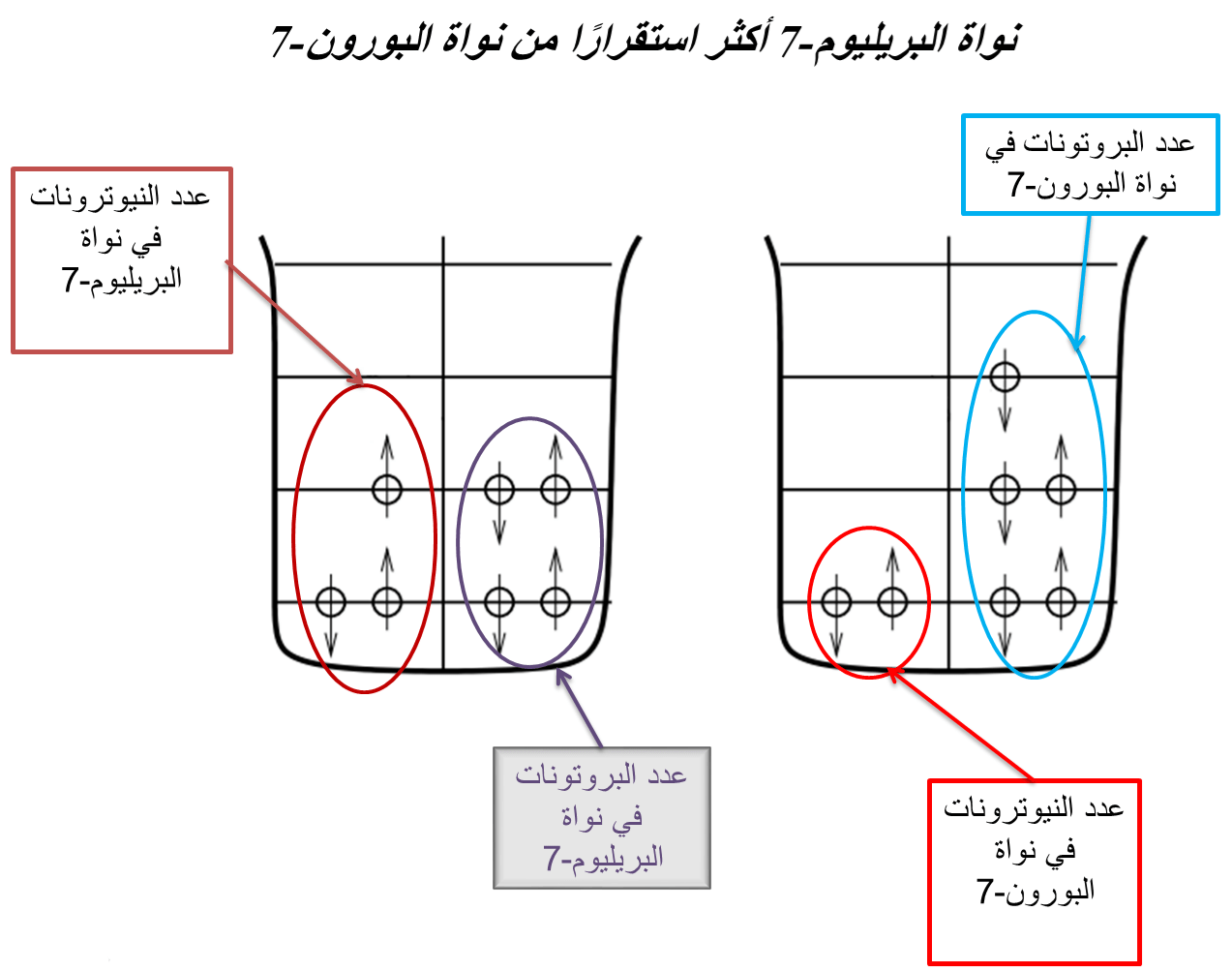
استقرار النواة
وللوصول إلى حالة الاستقرار، تسعَى النوى إلى الحصول على عدد متماثل من البروتونات والنيوترونات من خلال تحلل β، الذي يحول البروتونات إلى نيوترونات أو العكس. وهذا ما يفسر استقرار النوى الخفيفة التي تملك عددًا متساويًا من النيوترونات والبروتونات. بالنسبة للنوى الثقيلة (التي تملك عددًا كبيرًا من النويات)، فإن التنافر الذي يحدث بين شحنات البروتونات يضعف استقرار النواة. وللتغلب على هذا التنافر، تحتاج النواة لمزيد من النيوترونات لزيادة القوة النووية التي تربط النويات بعضها ببعض. لهذا، تنحو النوى الثقيلة لامتلاك نيوترونات أكثر من البروتونات. وتكون النوى أكثر استقرارًا أيضًا حين يكون عدد البروتونات زوجيًا وعدد النيوترونات زوجيًا حيث إن معظم النوى المستقرة إشعاعيًا، والتي تملك عددًا زوجيًا من النويات، يكون فيها عدد النيوترونات والبروتونات زوجيًا (155 نواة من بين 160 نواة موجودة في الطبيعة) [1].
نموذج قطرة السائل
في نموذج قطرة السائل، تم تشبيه نواة الذرة بقطرة ماء تتفاعل داخلها جزيئات الماء. ويقوم هذا النموذج على أساس قصر مدى القوى النووية، حيث تتفاعل كل نوية مع النويات التي تجاورها فقط، كما يحدث لجزيئات الماء مع بعضها البعض. بالإضافة إلى هذا، فإن النواة، كما قطرة الماء، غير قابلة للضغط، حيث تملك كثافة ثابتة. وتحافظ النواة على استقرارها بفضل طاقة الربط التي تبقي النويات مجتمعة داخل النواة، حيث تقابل طاقة الربط هذه حرارة التبخر عند قطرة الماء. فمن أجل تفكيك النواة، يجب منحها طاقة أكبر من طاقة الربط، وكذلك من أجل تفكيك قطرة الماء، يجب إعطاؤها طاقة تساوي حرارة التبخر [2].
صيغة الكتلة شبه التجريبية
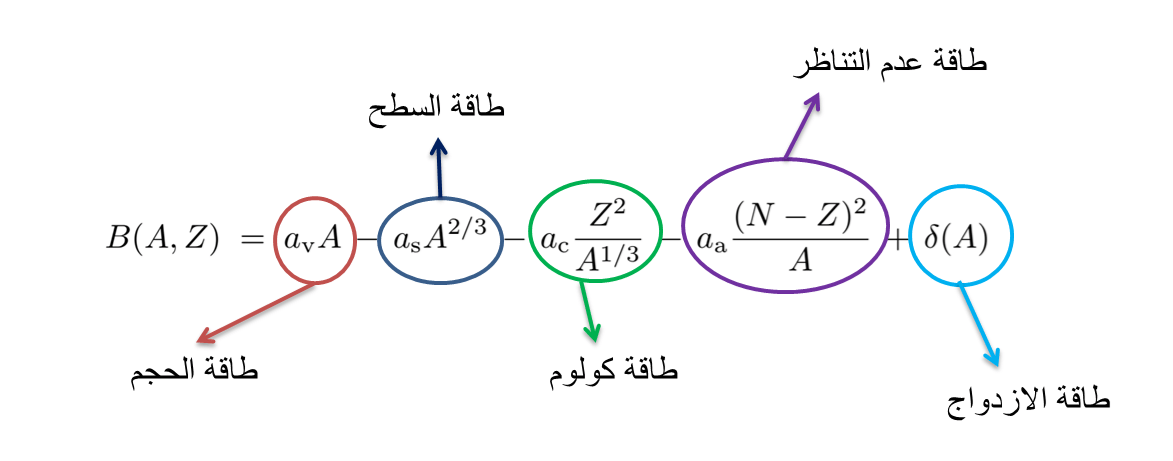
ويستعمَل نموذج قطرة السائل في حساب طاقة الربط لكل نوية -وهي طاقة الربط الكلية مقسومة على عدد نويات النواة، حيث قام «بيته-Bethe » و«فايزيكر-Weizsäcker» بوضع «صيغة الكتلة شبه التجريبية-semi-empirical mass formula » التي تُمَكِّن من حساب طاقة الربط. وتتكون هذه الصيغة من عدة معاملات تم تحديدها بحيث تكون طاقة الربط المحصل عليها بهذه الصيغة مساوية لتلك المأخوذة تجريبيا [1]. وتنقسم الصيغة إلى خمسة حدود:
- «طاقة الحجم- Volume Energy»، وتمثل تفاعل كل نوية مع ما يجاورها من نويات. وتتعلق هذه الطاقة بحجم النواة [1][2].
- «طاقة السطح-Surface Energy »، حيث تكون النويات الموجودة في سطح النواة أقل ارتباطًا من تلك التي تكون في المركز. ويرجع هذا لكون عدد النويات التي تجاور نويات السطح أقل من ذلك الذي عند نويات المركز، مما يسهم في إنقاص طاقة الربط. وهذا ما يفسر إشارة الناقص المرافقة لها [1][2].
- «طاقة كولوم-Coulomb Energy »، وتنتج عن تنافر البروتونات فيما بينها. مما يؤدي إلى إنقاص طاقة الربط.
- «طاقة عدم التناظر-Asymmetry Energy»، تفسر هذه الطاقة ارتفاع طاقة الربط عند النوى التي تملك عددا متماثلا من البروتونات والنيوترونات. ويكون هذا الحد مهما عند النوى الخفيفة. أما بالنسبة للنوى الثقيلة، فإن طاقة كولوم تطغى على هذه الطاقة. مما يؤدي إلى زيادة عدد النيوترونات في هذه النوى مقارنة بعدد البروتونات [1][2].
- «طاقة الازدواج-Pairing Energy»، وتعكس كون النوى ذات عدد بروتونات وعدد نيوترونات زوجي أكثر استقرارًا من غيرها [1][2].
نموذج غاز فيرمي
يعتمِد نموذج غاز فيرمي نموذج الجهد الثابت أساسا له، حيث يُشَبِّه النواة بكرة تحبس داخلها نوعين من الغازات: غاز البروتونات وغاز النيوترونات. وعلى عكس نموذج قطرة السائل التي ترتبط فيها طاقة النواة بخصائصها الهندسية، يعتمد نموذج غاز فيرمي على ميكانيكا الإحصاء الكمومي في حساب العوامل av وas وaa. ويعاني هذا النموذج من عدم دقته في تحديد طاقة الربط لدى النوى الخفيفة، حيث تكون أقل من تلك المقاسة تجريبيا [1].
نموذج القشرة
يتأسس نموذج القشرة، كما نموذج غاز فيرمي، على نموذج الجهد الثابت، حيث تخضع النويات لجهد ثابت. وتتموضع في هذا الجهد مستويات الطاقة التي تحتلها البروتونات والنيوترونات. وعلى عكس باقي النماذج، نجح نموذج القشرة في تفسير ظاهرة «الأعداد السحرية-magic numbers»، التي تكون فيها طاقة الربط في أقصى مستوياتها. وتعتبر النوى التي يكون عدد نيوتروناتها أو بروتوناتها مساويا لأحد هذه الأرقام (2،8،14،20،28،50،86،126) الأكثر استقرارا مقارنة ببقية النوى. وعلى غرار الفيزياء الذرية، حيث تكون الذرات في أقصى حالات الاستقرارعندما يكتمل عدد الإلكترونات في المدار الخارجي للذرة، فإن النوى الأكثر استقرارا هي تلك التي تملك مدارات ممتلئة، وهو ما يوافق الأعداد السحرية للبروتونات والنيوترونات [1].
في الختام، تبقَى هذه النماذج محاولات لتفسير ظاهرة النشاط الإشعاعي لبعض النوى. ولا يزال نموذج القشرة الأكثر نجاحا في ذلك.
المصادر
[1] Nuclear models and stability
[2] Principles of Radiation Interaction in Matter and Detection
سعدنا بزيارتك، جميع مقالات الموقع هي ملك موقع الأكاديمية بوست ولا يحق لأي شخص أو جهة استخدامها دون الإشارة إليها كمصدر. تعمل إدارة الموقع على إدارة عملية كتابة المحتوى العلمي دون تدخل مباشر في أسلوب الكاتب، مما يحمل الكاتب المسؤولية عن مدى دقة وسلامة ما يكتب.



التعليقات :